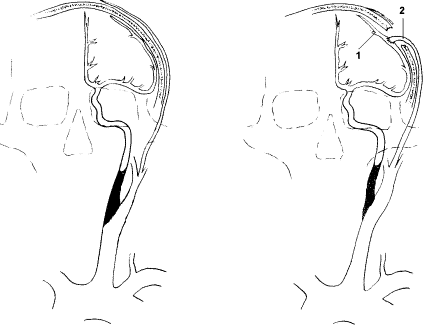
Рис.51. Схема выполнения экстракраниального- интракраниального
микроанастомоза (ЭИКМА) при окклюзии внутренней сонной
артерии.
1-ветвь поверхностной височной артерии, 2 - корковая ветвь средней
мозговой артерии.
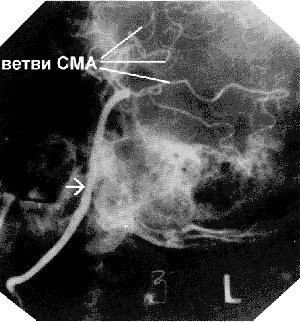
Рис.52. Правая каротидная ангиография: аутовенозный трансплантат
(стрелка) между ОСА и ветвью СМА.
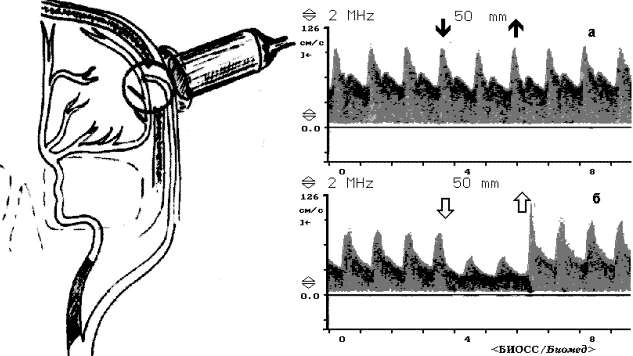
A
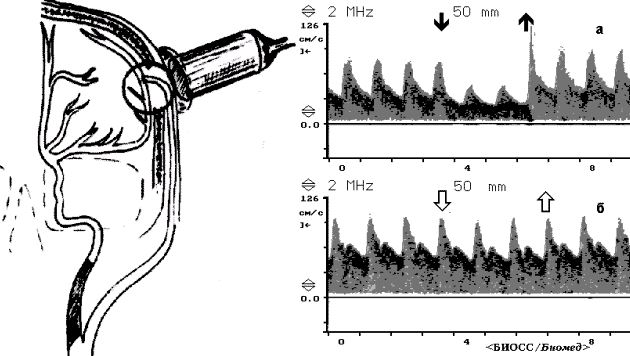
B
Рис.53. А. Схема расположения транскраниального датчика (слева) и
допплерограммы (справа) при I типе ЭИКМА : компрессия ПВА (a) не
приводит к изменению кровотока, компрессия контралатеральной ОСА
(b) - к редукции кровотока.
В. Схема расположения транскраниального датчика (слева) и
допплерограммы ( справа) при II типе ЭИКМА : компрессия ПВА (a)
приводит к редукции кровотока, компрессия контралатеральной ОСА
(b) не изменяет кровоток. (Cooperberg E.B.et al.Cardiovascular Surg.,1993 (c) - Vol.1- N.6)/P>
- состояние соединительных артерий Виллизиева круга (передних, задних соединительных артерий) и офтальмического анастомоза по критериям, подробно описанным в настоящем пособии;
- величина перфузионного мозгового резерва (ЦПР);
- тип функционирования ЭИКМА( гемодинамически значимый игемодинамически незначимый).
- состояние неврологического дефицита в баллах;
- состояние соединительных артерий Виллизиева круга, отдельно для передней соединительной артерии (ПСА), задней соединительной артерии (ЗСА) и для глазничного анастомоза (ГА);
- величина индекса ЦПР в см/сек/мм.рт.ст (ИЦПР) на стороне окклюзии ВСА;
- состояние ПА;
- объем очагового поражения мозговой ткани по данным КТ (в куб.см), в том числе локализация очага- поверхностная или глубинная;
- клиническая эффективность после создания ЭИКМА (выздоровление и улучшение состояния определялись как "положительный эффект", при отсутствии динамики - "отсутствие эффекта").
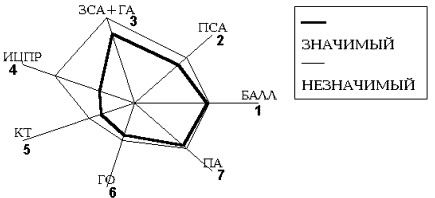
Рис.54. Прогноз гемодинамической эффективности ЭИКМА методом
многофакторного анализа.
1- степень сосудисто- мозговой недостаточности в баллах, 2- состояние
коллатерального кровообращения через ПСА, 3- состояние коллатерального
кровообращения через ЗСА и офтальмический анастомоз, 4- индекс цереб-
рального перфузионного резерва (ЦПР), 5 - величина инфаркта мозга по данным
компьютерной томографии, 6 - величина глубинного очага инфаркта мозга по
данным компьютерной томографии, 7- состояние позвоночных артерий по данным
ангиографии.( Куперберг Е.Б. с соавт. International symposium of
transcranial Doppler and intraoperative monitoring, St.Petersburg, 1995)
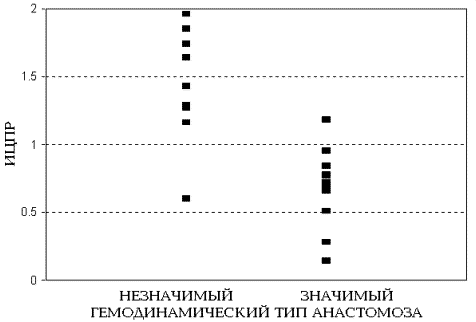
Рис.55. Сопоставление дооперационных индексов ЦПР с типами ЭИКМА
(Куперберг Е.Б. с соавт. International symposium of transcranial
Doppler and intraoperative monitoring, St.Petersburg, 1995)
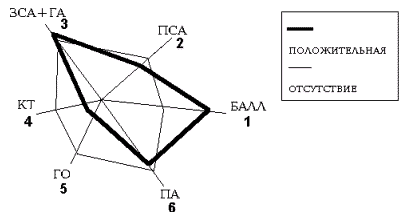
Рис.56. Прогноз клинической эффективности ЭИКМА методом
многофакторного анализа.
1- степень сосудисто- мозговой недостаточности в баллах, 2- состояние колла-
терального кровообращения через ПСА, 3- состояние коллатерального крово-обращения через ЗСА и офтальмический анастомоз, 4- величина инфаркта мозга по данным компьютерной томографии, 5- величина глубинного очага инфаркта мозга по данным компьютерной томографии, 6- состояние позвоночных артерий по данным ангиографии.
(Куперберг Е.Б. с соавт. International symposium of transcranial
Doppler and intraoperative monitoring, St.Petersburg, 1995)
- состояние мозговой гемодинамики у больных с окклюзией ВСА является определяющим фактором для гемодинамических показаний к созданию экстра-интракраниального анастомоза;
- создание ЭИКМА не показано при высоком перфузионном церебральном резерве;
- создание ЭИКМА показано при низком перфузионном церебральном резерве, при котором метод математического многофакторного анализа дает уверенный предоперационный прогноз гемодинамически значимого анастомоза;
- при сочетании экстракраниального поражения сонной артерии (стеноз наружной сонной артерии , окклюзия или стеноз общей сонной артерии) с окклюзией ВСА необходима первоочередная реконструкция этих сегментов для обеспечения нормальных гемодинамических условий для ЭИКМА.
- В то же время, достижение значимых положительных клинических результатов возможно лишь при легком неврологическом дефиците (ТИА, завершенный инсульт с легкими остаточными явлениями) при минимальном объеме поражения мозговой ткани по данным компьютерной томографии.
- Только совпадение условий гемодинамической и клинической эффективности и определяет совокупные показания к реваскуляризации мозга при хронической окклюзии ВСА. Следует еще раз подчеркнуть, что только тщательный отбор по гемодинамическим и клиническим признакам является наиболее верным путем определения показаний к этой операции. Транскраниальная допплерография является одним из опорных методов, позволяющих выполнить эту задачу.
Назад | Содержание | Вперед - В то же время, достижение значимых положительных клинических результатов возможно лишь при легком неврологическом дефиците (ТИА, завершенный инсульт с легкими остаточными явлениями) при минимальном объеме поражения мозговой ткани по данным компьютерной томографии.