ИСПОЛЬЗОВАНИЕ МЕТОДА КОНЕЧНЫХ ЭЛЕМЕНТОВ В ПОСТРОЕНИИ МОДЕЛИ РАДИОЧАСТОТНОЙ АБЛАЦИИ СЕРДЦА
А.С. Кравчук, Р.В.Фатеенко
Москва, ул. Стромынка, 20,
e-mail: roman4all@mail.ru
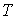 в области
в области 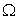 , занятой биотканью, и электрический потенциал
, занятой биотканью, и электрический потенциал 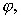 определеяемый потенциалам ина приложенных к границе
определеяемый потенциалам ина приложенных к границе 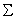 области
области 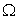 электродах. В общем случае распределение температуры подчиняется уравнению теплопроводности:
электродах. В общем случае распределение температуры подчиняется уравнению теплопроводности:
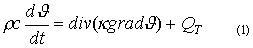
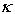 -теплопроводность,
-теплопроводность, 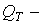 плотность источников (стоков) тепла;
плотность источников (стоков) тепла; 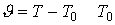 - комнатная температура,
- комнатная температура, 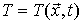 - текущая температура,
- текущая температура, 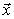 - пространственные координаты,
- пространственные координаты, 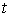 - время. Символ
- время. Символ 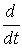 означает полную производную по времени, равную сумме локальной скорости изменения и конвективной. Этот объект используется в том случае, когда учитываются большие перемещения сердечной мышцы во время операции, а также гидродинамика потока крови в крупных сосудах. К уравнению (1) присоединяются граничные условия, которые приближенно можно взять в форме условий Дирихле:
означает полную производную по времени, равную сумме локальной скорости изменения и конвективной. Этот объект используется в том случае, когда учитываются большие перемещения сердечной мышцы во время операции, а также гидродинамика потока крови в крупных сосудах. К уравнению (1) присоединяются граничные условия, которые приближенно можно взять в форме условий Дирихле:
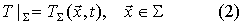
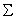 - граница области
- граница области 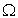 , занятой исследуемым материалом (органом), в которой работает уравнение (1). Необходимо также задать начальное условие:
, занятой исследуемым материалом (органом), в которой работает уравнение (1). Необходимо также задать начальное условие:
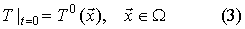 ,
,
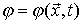 :
:
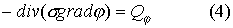 ,
,
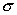 - электрическая проводимость биоткани, в данной задаче зависящая от координат и времени,
- электрическая проводимость биоткани, в данной задаче зависящая от координат и времени, 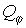 - плотность распределенных в области электрических зарядов.
- плотность распределенных в области электрических зарядов.
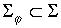 , к которой подсоединен задающий электрод, имеет вид:
, к которой подсоединен задающий электрод, имеет вид:
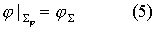
 - заданная функция координат и времени; на части поверхности
- заданная функция координат и времени; на части поверхности 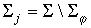 задается условие отсутствия тока через границу:
задается условие отсутствия тока через границу:
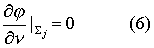
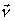 к границе
к границе 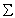 . Система уравнений (10-(6) оказывается связанной, поскольку плотность тепловых источников
. Система уравнений (10-(6) оказывается связанной, поскольку плотность тепловых источников 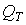 в исследуемом процессе определяется главным образом возникновением джоулева тепла, т.е. зависит от искомой функции
в исследуемом процессе определяется главным образом возникновением джоулева тепла, т.е. зависит от искомой функции  , входящей в уравнение (2). Если предположить, что не вся энергия электрического тока расходуется на нагревание, а только некоторая ее часть, пропорциональная джоулеву теплу, и что нельзя пренебречь переносом тепла вследствие кровотока, то:
, входящей в уравнение (2). Если предположить, что не вся энергия электрического тока расходуется на нагревание, а только некоторая ее часть, пропорциональная джоулеву теплу, и что нельзя пренебречь переносом тепла вследствие кровотока, то:
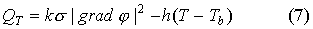
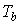 - температура крови,
- температура крови, 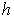 - коэффициент теплопередачи. Часть генерируемой электрическим током тепловой энергии расходуется на коагуляцию биоткани, так что коэффициент
- коэффициент теплопередачи. Часть генерируемой электрическим током тепловой энергии расходуется на коагуляцию биоткани, так что коэффициент 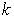 в формуле (7) не превосходит единицы.
в формуле (7) не превосходит единицы.
- Зенкевич О.С. Метод конечных элементов в технике. М.:Мир, 1975. 340с.
- Филатов А.Н. Методы усреднения в дифференциальных и интегро-дифференциальных уравнениях. Ташкент, ФАН, 1971. 279с.
- Panescu D., Whayne J.G., Fleischman S.D., Mirotznik M.S., Swanson D.K., Webster J.G. IEEE Trans. On Biomed. Engg. 1995, vol. 42, N 9, pp. 879-890.